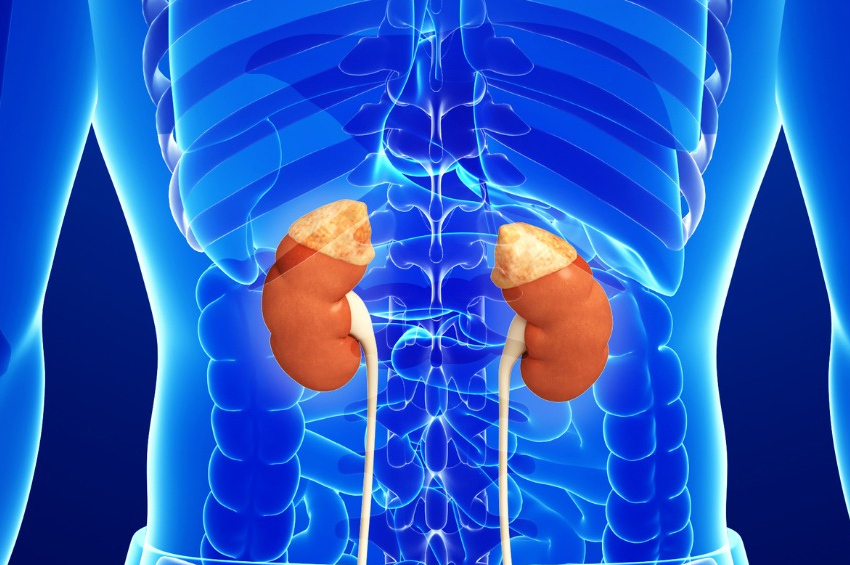
Adrenal kanser, adrenal bezlerde bir tümörün büyümesi ile karakterizedir. Bununla ilişkili belirti ve semptomlar, tümörün büyümesinin boyutuna ve doğasına göre önemli ölçüde değişebilir.
Haber Merkezi / Başlangıçta semptomlar oldukça belirsizdir, ancak genellikle tümör büyüdükçe ve karındaki yakın dokulara baskı yaptığında veya vücudun diğer bölgelerine yayıldıkça daha belirgin hale gelir.
Genel belirtiler
Adrenal kanserin göstergesi olabilecek belirti ve semptomlar, durumun ilk aşamalarında genellikle oldukça belirsizdir ve bu da tanıyı zorlaştırabilir. Bunlar;
- Karın içinde yumru
- Kronik ağrı (genellikle karın bölgesinde)
- Dolgunluk hissi
- Açıklanamayan kilo kaybı
- Ateş
Bununla birlikte, bunların oldukça genel olduğunu ve çok sayıda sağlık durumunun bir sonucu olarak ortaya çıkabileceğini belirtmek önemlidir. Bu nedenle adrenal kanserin nedenini belirlemek ve tanı koymak için ayırıcı tanı önemlidir. Bu süreçte genellikle kan testi, idrar testleri ve görüntüleme teknikleri gereklidir.
Fiziksel belirtiler
Adrenal bezin bir tümörü büyük bir boyuta gelebilse de, adrenal bezlerdeki tümörlerin çoğu iyi huyludur. Bununla birlikte, tümörün boyutu, iyi huylu olsalar bile mide gibi komşu organlara baskı yapabilir.
Tümörün boyutu hastalarda dolgunluk hissi yaşamasına neden olabilir. Bu iştah kaybına ve sonuç olarak açıklanamayan kilo kaybına neden olabilir.
Tümörün olduğu karın bölgesinde bir yumru veya kitle görülebilir. Bu, özellikle iyi huylu tümörleri olan hastalar tarafından bildirilen ilk işaret olabilir. Bu nedenle karın fizik muayenesi adrenal kanser tanısında önemli bir adımdır.
Hormonlar
Adrenal bezler, adrenalin ve kortizon gibi düzenleyici hormonların üretiminden sorumludur. Sonuç olarak, adrenal kanserin özellikleri, genellikle hormonların aşırı üretimi ve ilgili semptomlar gibi bu hormonlardaki dengesizliklerle yakından bağlantılıdır. Tümör tarafından salgılanan hormonun türü ilgili semptomları belirleyecektir.
Conn sendromu olarak da bilinen Conn hastalığı, aşırı aldosteron üretiminin neden olduğu adrenal kanser ile ilişkili bir durumdur. Bu, bazı durumlarda yaşamı tehdit edebilen hipokalemi, hipernatremi ve hipertansiyona yol açabilir.
Cushing sendromu, aşırı kortizol üretimini içeren adrenal kanser ile ilişkili bir durumdur. Bu, hipertansiyon, kilo alımı, anormal kilo dağılımı (şişkin yüz veya sırtta kambur), aşırı saç büyümesi, halsizlik ve yorgunluk gibi semptomlara yol açabilir.
Androjen veya östrojen hormonlarının aşırı üretimi, erkek ve dişilerin cinsel gelişimini etkileyebilir. Bu, çocuklarda erken ergenliğe veya yetişkinlerde cinsel özelliklerin değişmesine neden olabilir.
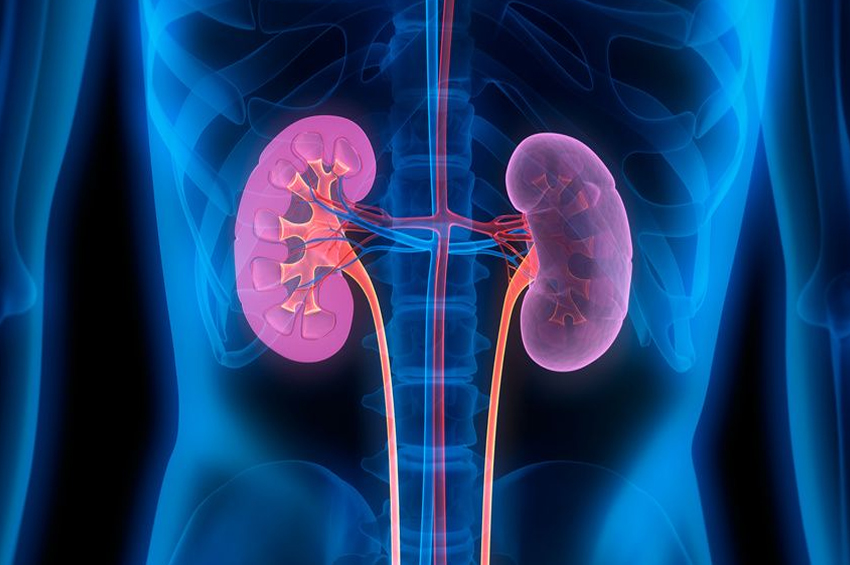
Teşhisi
Adrenal kanser tanısında birkaç önemli adım vardır. Başlangıçta, bir hasta genellikle adrenal kanseri gösterebilecek belirti veya semptomlarla başvurur. Bu, semptomların nedenini belirlemek için kan testleri, idrar testleri ve görüntüleme testlerini içeren bir araştırmayı gerektirir.
Bir tümör varsa, kanser büyümesinin doğasını belirlemek ve tedavi kararlarının alınmasına yardımcı olmak için görüntüleme testleri kullanılır.
Fiziki muayene
Tanının ilk aşamasında, adrenal kanserin yaygın semptomlarını belirlemeye yardımcı olan hedefe yönelik sorular da dahil olmak üzere eksiksiz bir ilaç geçmişi toplamak önemlidir. Bu, erkekler ve kadınlar için cinsel işlev ve kadınlar için adet döngüsü hakkında soruları içermelidir.
Ailesinde adrenal kanser öyküsü olan bireylerin bu durumdan etkilenme olasılığı daha yüksek olduğundan, benzer semptomlar yaşayan aile üyeleri hakkındaki sorular da konsültasyonda ele alınmalıdır.
Adrenal kanserin yaygın belirtilerini kontrol etmek için tanı sürecindeki bir sonraki aşama fizik muayenedir. Özellikle, bölgede bir kitle veya tümör kanıtı aramak için kapsamlı bir karın muayenesi yapılmalıdır.
Kan ve idrar testleri
Hem kan hem de idrar örnekleri alınmalı ve anormal hormon seviyeleri için analiz edilmelidir. Adrenal adenomları ve karsinomları olan hastalar, kan ve idrar testlerinde tespit edilebilen adrenal bezde üretilen hormonların üretimini artırma eğilimindedir. Ölçülmesi gereken önemli hormonlar şunlardır:
- Kortizol: Böbrek üstü bezindeki üretim artışına bağlı olarak artabilir.
- Aldosteron: Adrenal tümör tarafından hormon üretimi nedeniyle artabilir.
- Androjen hormonları: Adrenal tümör tarafından hormon üretimi nedeniyle artabilir.
- Östrojen: Adrenal tümör tarafından hormon üretimi nedeniyle artabilir.
Görüntüleme testleri
Görüntüleme testleri, adrenal kanser şüphesi olduğunda tümörün varlığını araştırmak için yararlıdır. Ayrıca tümörün yapısını ve kanserin yayılıp yayılmadığını da görselleştirebilirler. Görüntüleme teknikleri şunları içerebilir:
- Adrenal bezdeki tümörü ve kanserin karaciğere yayılıp yayılmadığını net bir şekilde görmek için bilgisayarlı tomografi (BT) taraması (doğruluk için tercih edilen yöntem).
- Adrenal bezdeki tümörü görselleştirmek ve iyi huylu tümörleri kötü huylu olanlardan ayırt etmek için manyetik rezonans görüntüleme (MRI).
- Adrenal bezdeki tümör kitlesini ve kanserin karaciğere yayılıp yayılmadığını görmek için ultrason.
- Pozitron emisyon tomografisi (PET), daha küçük kanser hücre gruplarını tespit etmek için tarama yapar, özellikle kanser böbreküstü bezinin dışına yayıldığında faydalıdır.
- Akciğerlere kanserin yayılmasını araştırmak için göğüs röntgeni.
Diğer tanı testleri
Görüntüleme testlerinden böbreküstü bezinde bir kitle görülüyorsa, önerilen hareket şekli tümörü çıkarmak için ameliyattır. Bir biyopsi bazen kullanılabilir, ancak biyopsi ile ilişkili olarak böbreküstü bezinin dışına yayılma riskinin artması nedeniyle nadiren tavsiye edilir.
Adrenal kanser tanısında kullanılabilecek başka bir prosedür laparoskopidir. Kanser büyümesini görmek için bir laparoskopun – ucunda bir video kamera bulunan ince, esnek bir tüp – hastanın yanına yerleştirilmesini içerir. Bu bazen tümörün daha net bir resmini elde etmek için ultrason gibi görüntüleme teknikleriyle birleştirilir.
Adrenal kanser, duruma yönelik tanı sürecinde kanserin ciddiyetine ve ilerlemesine göre evrelendirilebilir. Bu, tedavi kararlarını yönlendirmeye yardımcı olan ve birey için prognozun göstergesi olan önemli bir faktördür. Adrenal kanseri evrelemek için çeşitli sistemler vardır, ancak Dünya Sağlık Örgütü (WHO) tarafından geliştirilen, adrenal kanserin aşağıdaki gibi dört ana evre içerir:
- 1. evre: Tümörün çapı 5 santimetreden azdır ve adrenal bez içinde lokalizedir.
- 2. evre: Tümörün çapı 5 santimetreden fazladır ancak adrenal bez içinde bulunur.
- 3. evre: Kanserli büyüme, böbreküstü bezini çevreleyen yağ dokusuna yayıldı veya yakındaki lenf düğümlerine veya organlara yayıldı.
- 4. evre: Kanserli büyüme vücudun diğer organlarına veya bölümlerine yayılmıştır.
Tedavisi
Adrenal kanser teşhisinin ardından kullanılabilecek çeşitli tedavi seçenekleri vardır. Bu tekniklerin her biri, bazı durumlarda tercih edilirken bazılarında tercih edilmemesini sağlayacak benzersiz avantaj ve dezavantajlara sahiptir. Adrenal kanser nispeten nadir olduğundan, belirli bir vaka için en iyi tedavi seçeneklerini tartışmak için diğer endokrin uzmanlarıyla işbirliği yapmak faydalı olabilir.
Adrenal kanserin tedavisi tipik olarak cerrahlar, endokrinologlar, radyasyon onkologları, tıbbi onkologlar, hemşireler, psikologlar, sosyal hizmet uzmanları ve diğer sağlık profesyonellerini içerebilen çok disiplinli bir ekibi içerir.
Ameliyat
Adrenal kanser için en yaygın tedavi adrenalektomi veya adrenal bezin cerrahi olarak çıkarılmasıdır. Bu prosedürde, yakındaki lenf düğümleri gibi kanserin yayıldığı alanlar da dahil olmak üzere kanser mümkün olduğunca çıkarılır.
İşlem iki ana yolla yapılabilir: arkada kaburgaların altından veya karnın önünden bir kesi ile. Sırttaki kesi küçük tümörleri çıkarmak için kullanışlıdır ancak daha büyük tümörler için zor olabilir. Bu nedenle karın ön kısmından yapılan kesi pratikte en sık kullanılan yöntemdir.
Kanser karaciğer gibi vücudun diğer bölgelerine metastaz yapmışsa, bu ikincil tümörlerin cerrahi olarak çıkarılması da gerekebilir.
Küçük adrenal tümörler için, tümörü görmek ve çıkarmak için böbreküstü bezine bir laparoskop da yerleştirilebilir. Bu en yaygın olarak daha küçük tümörler için kullanılır ve iyileşme süresini azaltmaya yardımcı olur. Ancak nüks riskini azaltmak için tümörün tek parça halinde çıkarılması gerektiğinden daha büyük tümörler için kullanılamaz.
Radyasyon tedavisi
Odaklanmış yüksek enerjili radyasyon demetini içeren radyoterapi, adrenal bezdeki kanserli hücrelerin bölgesini hedeflemek için kullanılabilir. Bu genellikle cerrahi gibi diğer tekniklere ek olarak adjuvan tedavi olarak kullanılır.
Kullanılabilecek iki ana radyasyon tedavisi türü vardır: harici ışın radyasyon tedavisi ve dahili radyasyon tedavisi (brakiterapi).
Dış ışın radyasyon tedavisi, radyasyonu böbreküstü bezine yönlendirmek için vücudun dışında bir makine kullanır. Radyasyon genellikle yaklaşık 6 haftalık bir tedavi süresi boyunca haftada beş gün, günde bir veya iki kez uygulanır. Bu tip radyasyon tedavisinde radyasyonun tümöre ulaşmadan önce içinden geçtiği çevre doku da etkilenir. Bunu en aza indirmek için tedavi süreleri kısa tutulur, ancak bazı olumsuz etkiler yaşanabilir.
Brakiterapi olarak da bilinen dahili radyasyon tedavisi, vücudun içine tümörün yanına veya içine yerleştirilen küçük radyoaktif madde topakları kullanır. Bu genellikle birkaç gün vücutta bırakılır ve sonra çıkarılır. Radyasyonun lokalizasyonu, çevre dokulara maruz kalmayı azaltmaya yardımcı olur.
Kemoterapi
Adrenal kanserli hastalar için kemoterapi, intravenöz enjeksiyon veya oral ilaçlar yoluyla uygulanabilir. Bu teknik genellikle evre 4 adrenal kanserli hastalar için ayrılmıştır çünkü vücudun çeşitli bölgelerindeki kanser hücrelerini aynı anda yok etmeye yardımcı olabilir. Böbrek üstü bezinde bulunan kanser için genellikle cerrahi olarak çıkarılması tercih edilir.
Mitotan, adrenal bez hormon üretimini engelleyebildiği ve kanser hücrelerini yok ettiği için adrenal bez için kullanılan yaygın bir kemoterapötik ajandır. Özellikle aşırı hormon üretiminin neden olduğu kanserler için faydalıdır. Diğer kemoterapötik ajanlar gibi bu süreçte bazı sağlıklı hücreleri de yok eder.
Genellikle mitotan ile kombinasyon halinde kullanılan diğer kemoterapötik ajanlar şunlardır:
- Sisplatin
- Doksorubisin
- Etoposid
- Streptozosin
- Paklitaksel
- 5-florourasil
- Vinkristin
Diğer ilaçlar
Adrenal kanser tedavisinde, öncelikle tümörle ilgili hormonların üretimini azaltmak için kullanılabilecek başka ilaçlar da vardır. Bunlar;
- Adrenal steroid hormonlarının üretimini azaltmak için Ketokonazol ve Metirapon
- Aldosteronun etkilerini azaltmak için spironolakton
- Kortizolün etkilerini azaltmak için mifepriston
- Östrojen etkilerini engellemek için Tamoxifen, Toremifene ve Fulvestrant
Dikkat: Sayfa içeriği sadece bilgilendirme amaçlıdır.