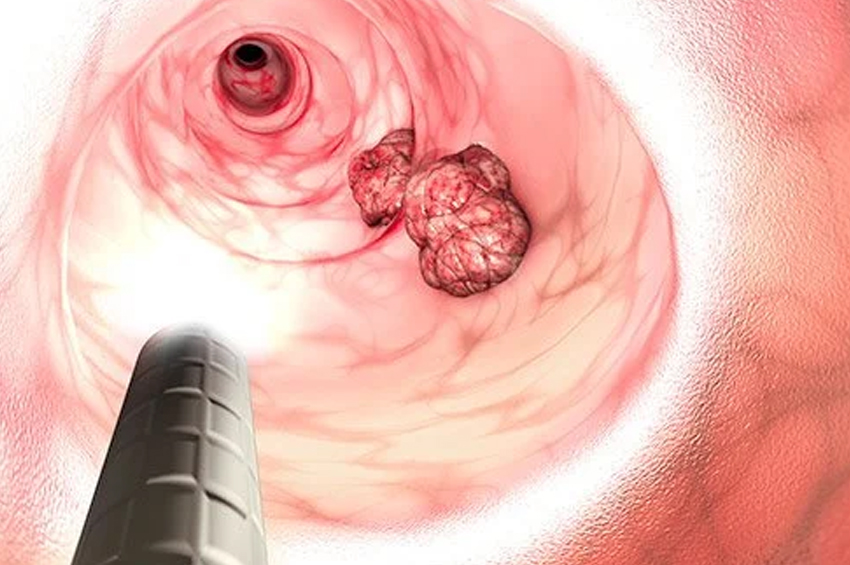
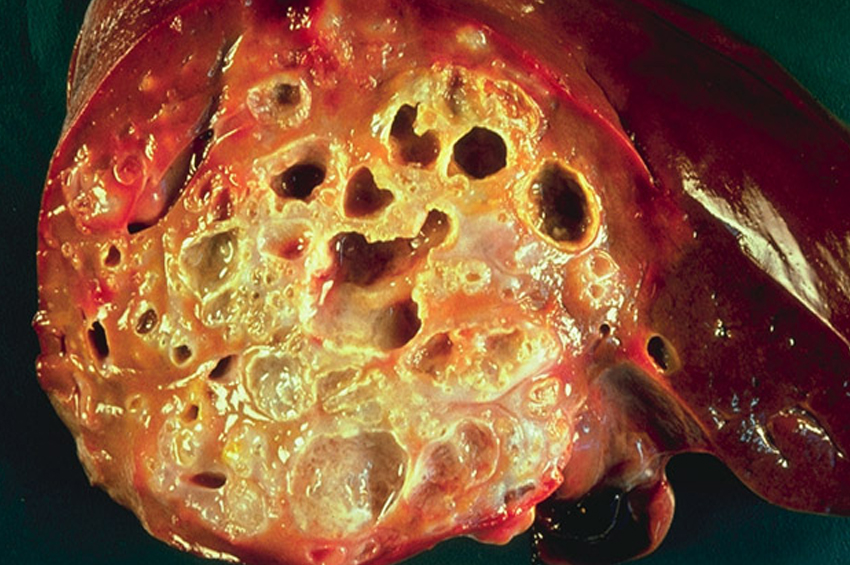
Anüs, kalın bağırsağın vücudun dışına açılan en alt kısmıdır. Dışkı ve vücut atıkları bu açıklıktan dışarı atılır. Anüsü kaplayan hücreler, düzleşmiş ve cilt hücreleri gibi görünen hücrelerden oluşur. Bunlara skuamöz hücreler denir.
Haber Merkezi / Anüs ve rektumun birleştiği yerdeki alana geçiş bölgesi denir. Burada anüsün astarı değişir ve hem skuamöz hem de glandüler hücrelerden oluşur. Glandüler hücreler, mukus dahil çeşitli sıvılar salgılayan hücrelerdir.
Bu, dışarıya atılacak atıkların düzgün geçişine yardımcı olur. Anüs ile rektumu ayıran bu çizgiye dentat çizgi denir. Anüsün açılmasını düzenleyen iki sfinkter veya kapı vardır.
Türleri
En yaygın anal kanser türlerinden biri skuamöz hücreli kanserdir (tüm anal kanserlerin %80’i). Birkaç farklı skuamöz hücreli anal kanser türü vardır. Bazen epidermoid kanserler olarak adlandırılırlar.
Daha nadir bir tip, geçiş bölgesindeki glandüler hücreleri etkileyen adenokarsinomdur. Diğer anal kanser türleri arasında bazal hücreli karsinom ve melanom bulunur.
Bazen anüsün yüzey tabakasındaki hücreler kanser hücrelerine benziyor ancak daha derindeki tabakalara doğru büyümediler. Bu karsinoma in situ olarak bilinir. Bowen hastalığı olarak da adlandırılabilir.
Nedenleri ve risk faktörleri
Anal kanser nadirdir. Kadınlar erkeklerden daha sık etkilenir. Risk faktörlerinden bazıları, İnsan papilloma virüsü (HPV) enfeksiyonlarını içerir. 100’den fazla farklı HPV türü vardır. Bunlardan bazıları cinsel temas yoluyla yayılabilir.
Anal kanser teşhisi konanların yaklaşık %80’inde HPV enfeksiyonu kanıtı vardır. Diğer risk faktörleri arasında yaşlanma, cinsel yolla bulaşan hastalık varlığı, sigara kullanımı, bağışıklık yetersizliği vb. sayılabilir.
Belirtileri
Anal kanserin semptomları, basur (hemoroid) veya anal fissür gibi diğer anal bozukluklara benzer. Bazı bireyler (yaklaşık %20’si) herhangi bir semptom göstermeyebilir.
Belirtilerden bazıları şunlardır:
- Rektal kanama
- Anüsten mukus akıntısı
- Anüs çevresinde ağrı
- Bağırsakları boşalttıktan sonra anüste bir yumru hissi ve eksik tahliye hissi
- Anüs çevresinde yığın şeklinde görünen küçük topaklar
- Bağırsakları veya fekal inkontinansı kontrol etmede zorluk
- Kasıkta şişmiş lenf düğümlerini gösteren yumru(lar)
- Anemi ve belirtileri
Tarama ve teşhis
Tarama, herhangi bir semptom görülmeden önce bir hastalığın erken evrelerini tespit etmek için büyük duyarlı ancak sağlıklı popülasyonların test edilmesi anlamına gelir. Testin doğru, güvenilir olması ve yanlış pozitif sonuç vermemesi gerekir. Şu anda anal kanser için böyle uygun tarama testleri bulunmamaktadır.
Anal kanser teşhisi şunları içerir:
- Dijital rektal muayene; Bu, bir eldiveni ve parmağını nazikçe anüse sokan ve topakları hisseden cerrah tarafından gerçekleştirilir. Kadınlar ayrıca anüsteki herhangi bir yumruyu tespit etmek için vajinalarının iç muayenesine de sahip olabilirler.
- Kitle biyopsisi; Tümörden küçük bir doku örneği alınır. Daha sonra bir lam üzerine sabitlenir ve uygun boyalarla boyandıktan sonra mikroskop altında incelenir. Lokal veya genel anestezi altında biyopsi yapılabilir. Hücresel görünüm, daha yüksek derecede doğrulama ile anal kanseri tespit etmeye yardımcı olabilir.
- Görüntüleme çalışmaları; CT (bilgisayarlı tomografi) taraması, kanserin yayılımını ve tam boyutunu tespit etmek için reçete edilir. MRI (manyetik rezonans görüntüleme) taraması, daha ayrıntılı bir görüntüleme çalışmasıdır. Yayılma ve diğer kanser odaklarını/odaklarını kontrol etmek için tüm karın MRG’si önerilir. Vücudun farklı bölgelerindeki kanser hücrelerinin aktivitesini tespit etmek ve kanseri tanımlamak için bir PET-CT taraması veya bir Endoanal ultrason taraması da kullanılabilir.
Anal kanserin evrelenmesi ve derecelendirilmesi; Laboratuvar ve görüntüleme çalışmaları yapıldıktan sonra kanser evrelendirilir ve derecelendirilir.
Düşük dereceli bir kanser, kanser hücrelerinin normal hücrelere çok benzediği ve dolayısıyla yavaş büyüdüğü ve daha az agresif olduğu anlamına gelir. Yüksek dereceli kanser hücreleri normal hücrelerden çok farklıdır ve bu nedenle agresif ve hızlı büyürler. Bunların yayılma olasılığı daha yüksektir.
Bir kanserin evresi, boyutunu ve orijinal bölgesinin ötesine yayılıp yayılmadığını tanımlar. Bu, en uygun tedaviye karar vermede yardımcı olur ve sonucu veya prognozu tahmin eder.
- 1. evre, kanser sadece anusu etkiler ve boyutu 2 cm’den (¾ inç) küçüktür. Sfinkter kasına yayılmaya başlamamıştır.
- 2. evre, kanserin boyutu 2 cm’den (¾ inç) büyüktür, ancak henüz yakındaki lenf düğümlerine veya vücudun diğer bölgelerine yayılmamıştır.
- 3. evre, kanserde rektum yakınındaki lenf bezlerine veya mesane veya vajina gibi yakın organlara veya kasık ve pelvisteki lenf bezlerine yayılır.
- 4. evre, anal kanserde kanser, karındaki lenf düğümlerine veya karaciğer gibi vücudun diğer bölgelerine yayılmıştır.
Epidemiyolojisi
Anal kanserler çok yaygın değildir, ancak kadınlar bu kansere erkeklerden daha yatkındır. Anal kanserler, kolon veya rektum kanserinden çok daha az yaygındır.
Tedavisi
Anal kanser için ana tedavi türü, hem radyasyon tedavisi hem de kemoterapinin bir kombinasyonudur. İki tedavi normalde aynı anda verilir. Buna kemoradyasyon denir. Kombine tedavi genellikle çok başarılıdır. Küçük tümörler için cerrahi faydalı olabilir.
Radyasyon tedavisi
Radyasyon tedavisi için kanser hücrelerini yok etmek için yüksek enerjili x ışınları kullanılır. Bu ışınlar, büyük bir X ışını benzeri makine kullanılarak vücudun dışından kansere yönlendirilir.
Bunun için hastanın sık sık tesisi ziyaret etmesi gerekir. Tedavi genellikle 4-6 hafta boyunca hafta içi her gün birkaç dakika verilir. Buna harici radyoterapi denir.
Radyasyon tedavisinin yaygın yan etkileri şunlardır:
- İshal
- Aşırı gaz ve şişkinlik
- Radyasyon alanı çevresinde deri döküntüleri ve yanıklar
- Saç kaybı
- Vajinal ve anal kuruluk
- Tükenmişlik
- Kısırlık
- İktidarsızlık
- Erken menopoz vb.
Kemoterapi
Kemoterapi için kanser hücrelerini öldürmek için anti kanser ilaçları kullanılır. Anal kanseri tedavi etmek için yaygın olarak kullanılan ilaçlar arasında mitomisin, kapesitabin ve fluorourasil (5FU) bulunur.
Kemoterapi, aşağıdakiler de dahil olmak üzere çeşitli yan etkilere neden olabilir:
- Anemi
- Düşük beyaz kan hücresi sayımı nedeniyle enfeksiyon eğilimi
- Düşük trombosit sayısı nedeniyle kanama riskleri
- Saç kaybı
- İshal
- Kusma
- Mide bulantısı
- Tükenmişlik
- İştah kaybı
- Ağız ülseri vb.
Ameliyat
Küçük anal kanserler için cerrahi yararlıdır. Ameliyat türleri, tümörün lokal rezeksiyonu içerir. Ameliyat, anüsün sadece kanser hücrelerini içeren bölgesini çıkarır. Anal sfinkter korunur ve bağırsak fonksiyonu normal kalır.
Daha kapsamlı bir ameliyat, hem anüsün hem de rektumun çıkarıldığı abdominoperineal rezeksiyondur. Operasyon, dışkıyı yapay bir açıklıktan boşaltmaya yardımcı olan kalıcı bir kolostomi gerektirir.
Dikkat: Sayfa içeriği sadece bilgilendirme amaçlıdır.